関連記事一覧

国立大学病院過去最大285億円の赤字―大鳥会長「このままなら間違いなく潰れる」
★
★
★
★
★
3
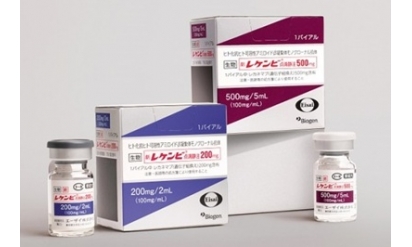
AD治療薬「レケンビ」薬価15%引下げへ─中医協が費用対効果評価案を了承
★
★
★
★
★
3

理解されにくい月経・PMSの症状は「イライラ感」「情緒不安定」「眠気」─ツムラ調査
★
★
★
★
★
3

SOMPOケア、インド人材受け入れ開始 段階的に拡大 年100人規模で外国人材の中核へ
★
★
★
★
★
3

今年上半期の訪問介護の倒産、過去最多に 中堅規模にも波及 進む業界の地盤沈下
★
★
★
★
★
3

オンプレ型電子カルテ導入施設にクラウド型への移行を促す─医療DX推進で厚労省
★
★
★
★
★
3