メディカルサポネット 編集部からのコメント厚生労働省は骨粗鬆症に用いる「イベニティ」(ロモソズマブ)について添付文書改訂を日本製薬団体連合会に対し指示しました。過去1年以内の心血管系事象の既往がある患者への投与は避ける旨が追記されます。 |
厚生労働省は9月6日付で、日本製薬団体連合会に対し、骨折の危険性が高い骨粗鬆症に用いる「イベニティ」(一般名:ロモソズマブ)などの添付文書改訂を指示する通知を発出した(下掲)。
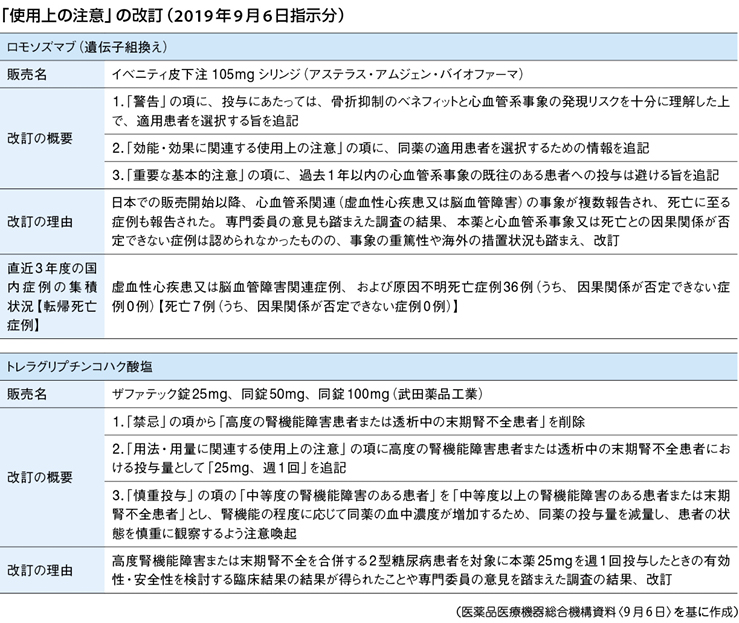
イベニティでは、「警告」の項に、骨折抑制のベネフィットと心血管系事象の発現リスクを十分に理解した上で、適用患者を選択する旨を追記。同薬による治療中は、心血管系事象の発現がないか注意深く観察するとともに、徴候や症状が認められた場合には速やかに医療機関を受診するよう指導することを求めている。「重要な基本的注意」の項には、過去1年以内の心血管系事象の既往がある患者への投与は避ける旨を追記する。
2型糖尿病に用いる「ザファテック」(一般名:トレラグリプチンコハク酸塩)では、「禁忌」の項から「高度の腎機能障害患者または透析中の末期腎不全患者」を削除。同患者に対する投与量として「25mg、週1回」を追記した。投与中は患者の状態を慎重に観察するよう注意喚起している。高度腎機能障害患者、末期腎不全患者における低血糖や感染症を含めた同薬の安全性については、特定使用成績調査(高度腎機能障害または末期腎不全を合併する2型糖尿病患者での長期使用に関する調査)などで情報収集するとしている。
出典:Web医事新報